« Guide 04-06-02 » : différence entre les versions
mAucun résumé des modifications |
mAucun résumé des modifications |
||
| Ligne 4 : | Ligne 4 : | ||
{{Bandeau Source du contenu Fertilisation 2022}} | {{Bandeau Source du contenu Fertilisation 2022}} | ||
<p class="lead"> En révélant la richesse du sol en éléments nutritifs, le pH et le taux de matière organique, les analyses de sol permettent une fertilisation rationnelle. Elles sont utiles et nécessaires, mais sont loin d’apporter toute l’information, notamment en ce qui concerne la qualité de la matière organique et l’apport d’azote du sol. Idéalement, pour bien élaborer un plan de fertilisation, il faut jumeler l’interprétation de l’analyse de sol à un examen physique à l’aide de l’étude du profil de sol. En effet, la structure du sol et l’état du drainage sont souvent plus importants que la richesse du sol en éléments nutritifs pour la croissance des plantes. Pour plus d’information sur l’évaluation de l’état des sols, voir le document ''[https://www.craaq.qc.ca/Publications-du-CRAAQ/les-profils-de-sol-agronomiques/p/PAUT0034 Les profils de sol agronomiques, un outil de diagnostic de l’état des sols]'' (Weill, 2009b) et la vidéo ''[https://www.youtube.com/watch?v=h8fh47sHzd4 Comment réaliser un profil agropédologique]''. </p> | <p class="lead"> En révélant la richesse du sol en éléments nutritifs, le pH et le taux de matière organique, les analyses de sol permettent une fertilisation rationnelle. Elles sont utiles et nécessaires, mais sont loin d’apporter toute l’information, notamment en ce qui concerne la qualité de la matière organique et l’apport d’azote du sol. '''Idéalement, pour bien élaborer un plan de fertilisation, il faut jumeler l’interprétation de l’analyse de sol à un examen physique à l’aide de l’étude du profil de sol.''' En effet, la structure du sol et l’état du drainage sont souvent plus importants que la richesse du sol en éléments nutritifs pour la croissance des plantes. Pour plus d’information sur l’évaluation de l’état des sols, voir le document ''[https://www.craaq.qc.ca/Publications-du-CRAAQ/les-profils-de-sol-agronomiques/p/PAUT0034 Les profils de sol agronomiques, un outil de diagnostic de l’état des sols]'' (Weill, 2009b) et la vidéo ''[https://www.youtube.com/watch?v=h8fh47sHzd4 Comment réaliser un profil agropédologique]''. </p> | ||
Il | == Études pédologiques == | ||
Il est toujours bon de consulter les cartes et les rapports pédologiques pour avoir une idée générale du type de sol avec lequel on travaille ([http://www.info-sols.ca/ Info-sol]; [https://sis.agr.gc.ca/siscan/publications/surveys/pq/index.html Agriculture et Agroalimentaire Canada]; [https://www.irda.qc.ca/fr/services/protection-ressources/sante-sols/information-sols/etudes-pedologiques/ IRDA]). En plus de la [https://www.irda.qc.ca/fr/services/protection-ressources/sante-sols/information-sols/ documentation sur les sols du Québec], plusieurs [https://www.irda.qc.ca/fr/publications/?t=1408&r=2232#documents fiches synthèses sur les séries de sol] ont été réalisées par l’Institut de recherche et de développement en agroenvironnement (IRDA). | |||
Au Québec, la méthode d’analyse des éléments nutritifs pour les sols de | == Échantillonnage == | ||
Il existe divers protocoles d’échantillonnage de sol : échantillonnage traditionnel ([https://www.craaq.qc.ca/Publications-du-CRAAQ/guide-de-reference-en-fertilisation-2e-edition-actualisee/p/PSOL0104-PDF CRAAQ, 2013, p. 40 à 45]; [http://www.omafra.gov.on.ca/french/engineer/facts/06-032.htm OMAFRA]; [https://www2.gnb.ca/content/dam/gnb/Departments/10/pdf/Agriculture/echantillonageSol.pdf Gouvernement du Nouveau-Brunswick]) ou [https://www.craaq.qc.ca/Publications-du-CRAAQ/echantillonnage-conventionnel-des-sols-agricoles-au-quebec-%E2%80%93-de-la-planification-a-l_envoi-au-laboratoire/p/PSOL0102-PDF géoréférencé]. L’échantillon doit être représentatif des types de sols pour ajuster la fertilisation par zone. Ainsi, les secteurs homogènes devraient être identifiés en fonction de la série de sol, la granulométrie, l’égouttement, la topographie ou les pratiques agricoles passées. La profondeur d’échantillonnage visée est de 18 cm. Il est suggéré de prélever une quinzaine de sous-échantillons par champ qui seront mélangés pour l’envoi au laboratoire. L’échantillon envoyé au laboratoire ne devrait pas peser plus de 1 kg (300 ml sont suffisants). Il est aussi intéressant d’obtenir des analyses du sous-sol (couche juste au-dessous de la couche de labour, soit à plus de 18 cm de profondeur). Cette partie du sol est peu affectée par la fertilisation et le chaulage. Une telle analyse permet cependant de vérifier si le sol est naturellement acide et d’évaluer ses réserves naturelles en phosphore, en potassium et en magnésium. | |||
== Analyse en laboratoire == | |||
Au Québec, la méthode d’analyse des éléments nutritifs pour les sols de champ est l’extraction Mehlich III<ref>La méthode Mehlich-III a été développée en 1984 par l'américain Adolph Mehlich, un scientifique des sols de la Caroline du Nord ([https://edis.ifas.ufl.edu/publication/SS620 Mylavarapu, 2020]). Elle fut implantée au Québec en 1989 par le Service de recherches en sols du ministère de l'Agriculture, des Pêcheries et de l'Alimentation du Québec (MAPAQ). Elle permet d'extraire plusieurs éléments nutritifs '''pour les sols dont le pH est acides à neutres''', ce qui correspond à la plupart des sols agricoles du Québec ([https://www.agrireseau.net/legumeschamp/blogue/106877/au-dela-des-grilles-regionales-de-reference-en-fertilisation-il-y-a-la-complexite-d_un-ecosysteme-agricole-local Parent, 2021]). La solution Mehlich-III, un acide faible, a été élaboré de façon à imiter les conditions d'extraction des éléments nutritifs dans la zone racinaire. Lors de l'analyse, la solution est versée sur l'échantillon de sol qui se trouve dans un entonnoir. Le liquide qui en ressort est analysé pour en connaître le contenu en divers éléments (P, K, Ca, Mg, Na, Al, Cu, Zn, Mn et Fe). La solution extractive Mehlich III se compose de CH<sub>3</sub>COOH, NH<sub>4</sub>NO<sub>3</sub>, NH<sub>4</sub>F, HNO<sub>3</sub> et EDTA ([https://www.environnement.gouv.qc.ca/milieu_agri/agricole/guide1.htm MELCCFP, s. d.])</ref>. Les résultats d’analyse (P<sub>2</sub>O<sub>5</sub>, K<sub>2</sub>O, Ca, Mg et autres), présentés de façon détaillée dans les prochaines sections, doivent être interprétés à l'aide du [https://www.craaq.qc.ca/Publications-du-CRAAQ/r?q=%22Guide%20de%20r%C3%A9f%C3%A9rence%20en%20fertilisation%2C%202e%20%C3%A9dition%22 ''Guide de référence en fertilisation''] (CRAAQ. 2013). Pour un résumé des références, voir [http://blog.ac-versailles.fr/formationcapa/public/MP2/Interpretation_AnalyseSol_.pdf ''Le guide pour l'interprétation d'une analyse de sol'']. | |||
Pour les sols en serre (non traités dans ce chapitre) des analyses SSE (Soil Saturated Extract) sont aussi utilisées. Celles-ci donnent la quantité d’éléments présents dans la solution du sol qui sont immédiatement disponibles aux plantes. Ces valeurs peuvent varier de jour en jour et représentent une petite fraction des valeurs données par l’analyse de sol standard. Cette dernière indique plutôt les éléments disponibles pour la plante à moyen terme. | Pour les sols en serre (non traités dans ce chapitre) des analyses SSE (Soil Saturated Extract) sont aussi utilisées. Celles-ci donnent la quantité d’éléments présents dans la solution du sol qui sont immédiatement disponibles aux plantes. Ces valeurs peuvent varier de jour en jour et représentent une petite fraction des valeurs données par l’analyse de sol standard. Cette dernière indique plutôt les éléments disponibles pour la plante à moyen terme. | ||
Version du 2023-01-18 à 07:41:12
Le contenu qui suit est issu de :
Oeuvre originale : Weill, A. et Duval, J. (2009). Guide de gestion globale de la ferme maraîchère biologique et diversifiée. Équiterre.
Révision : Weill, A., Legault, G., Bergeron, E., Méthé, A., La France, D., St-Arnaud, R., Roy, J., Khanna, R. et Gagné, G. (2022).
Pour contribuer, vous pouvez commenter (en bas de page) ou démarrer une discussion sur le sujet (bouton « … » en haut à droite). Pour modifier le contenu, veuillez contacter les auteur·rices ou écrire à l’équipe du WM. Pour suivre l'évolution de cette page, sélectionnez l'option à cet effet dans le menu "...".
En révélant la richesse du sol en éléments nutritifs, le pH et le taux de matière organique, les analyses de sol permettent une fertilisation rationnelle. Elles sont utiles et nécessaires, mais sont loin d’apporter toute l’information, notamment en ce qui concerne la qualité de la matière organique et l’apport d’azote du sol. Idéalement, pour bien élaborer un plan de fertilisation, il faut jumeler l’interprétation de l’analyse de sol à un examen physique à l’aide de l’étude du profil de sol. En effet, la structure du sol et l’état du drainage sont souvent plus importants que la richesse du sol en éléments nutritifs pour la croissance des plantes. Pour plus d’information sur l’évaluation de l’état des sols, voir le document Les profils de sol agronomiques, un outil de diagnostic de l’état des sols (Weill, 2009b) et la vidéo Comment réaliser un profil agropédologique.
Études pédologiques
Il est toujours bon de consulter les cartes et les rapports pédologiques pour avoir une idée générale du type de sol avec lequel on travaille (Info-sol; Agriculture et Agroalimentaire Canada; IRDA). En plus de la documentation sur les sols du Québec, plusieurs fiches synthèses sur les séries de sol ont été réalisées par l’Institut de recherche et de développement en agroenvironnement (IRDA).
Échantillonnage
Il existe divers protocoles d’échantillonnage de sol : échantillonnage traditionnel (CRAAQ, 2013, p. 40 à 45; OMAFRA; Gouvernement du Nouveau-Brunswick) ou géoréférencé. L’échantillon doit être représentatif des types de sols pour ajuster la fertilisation par zone. Ainsi, les secteurs homogènes devraient être identifiés en fonction de la série de sol, la granulométrie, l’égouttement, la topographie ou les pratiques agricoles passées. La profondeur d’échantillonnage visée est de 18 cm. Il est suggéré de prélever une quinzaine de sous-échantillons par champ qui seront mélangés pour l’envoi au laboratoire. L’échantillon envoyé au laboratoire ne devrait pas peser plus de 1 kg (300 ml sont suffisants). Il est aussi intéressant d’obtenir des analyses du sous-sol (couche juste au-dessous de la couche de labour, soit à plus de 18 cm de profondeur). Cette partie du sol est peu affectée par la fertilisation et le chaulage. Une telle analyse permet cependant de vérifier si le sol est naturellement acide et d’évaluer ses réserves naturelles en phosphore, en potassium et en magnésium.
Analyse en laboratoire
Au Québec, la méthode d’analyse des éléments nutritifs pour les sols de champ est l’extraction Mehlich III[1]. Les résultats d’analyse (P2O5, K2O, Ca, Mg et autres), présentés de façon détaillée dans les prochaines sections, doivent être interprétés à l'aide du Guide de référence en fertilisation (CRAAQ. 2013). Pour un résumé des références, voir Le guide pour l'interprétation d'une analyse de sol.
Pour les sols en serre (non traités dans ce chapitre) des analyses SSE (Soil Saturated Extract) sont aussi utilisées. Celles-ci donnent la quantité d’éléments présents dans la solution du sol qui sont immédiatement disponibles aux plantes. Ces valeurs peuvent varier de jour en jour et représentent une petite fraction des valeurs données par l’analyse de sol standard. Cette dernière indique plutôt les éléments disponibles pour la plante à moyen terme.
Note : Au Québec, les résultats d’analyse pour le phosphore, le potassium, le magnésium et le calcium sont indiqués en kg/ha. Ailleurs dans le monde, on utilise plutôt les ppm (parties par million). La conversion est la suivante : 1 kg/ha = 1 ppm x 2,24.
Sol minéral et sol organique
L’interprétation des analyses de sol décrite ci-dessous concerne les sols minéraux. De façon générale, les sols sont divisés en plusieurs ordres ayant des caractéristiques physiques et chimiques spécifiques (podzols, gleysols, brunisol, sols organiques etc.) Pour plus d’information à ce sujet, voir le Guide de référence en fertilisation (CRAAQ, 2013, p. 7-22). En ce qui a trait à la fertilisation, il est important de distinguer les sols organiques des autres grands ordres de sol qui eux, sont minéraux. Les sols organiques contiennent plus de 30% de matière organique sur une épaisseur d’au moins 40 à 60 cm.
Le complexe argilo-humique et la capacité d’échange cationique
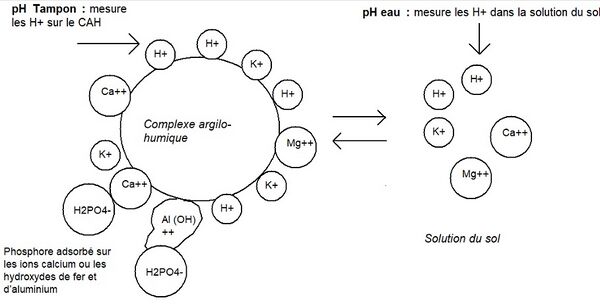
Le complexe argilo-humique (CAH) est constitué d’argile et de matière organique. Ces deux fractions sont chargées négativement et sont liées ensemble principalement par le calcium qui est positif (Figure 1). Globalement, le complexe est chargé négativement ce qui lui permet de retenir les cations (éléments positifs comme le calcium, le magnésium, le potassium et l’hydrogène). Dans la figure 1, chaque cation est associé à un site négatif qui se trouve sur le complexe.
La capacité d’échange cationique (CEC) est constituée par le nombre de sites négatifs qui se trouvent sur le complexe.
Le pH
pH eau et pH tampon
Le pH, ou potentiel hydrogène, permet de mesurer l’acidité du sol. L'acidité du sol est due aux ions hydrogènes (H+) qui se trouvent soit dans la solution du sol, soit sur le complexe argilo-humique (CAH) (Figure 1) .
Le pH eau mesure la quantité d'ions hydrogène dans la solution du sol. Le pH eau ne permet pas de déterminer les quantité de chaux à ajouter.
Le pH tampon est un indicateur de l’acidité potentielle du sol. Il mesure la quantité d'ions hydrogène sur le complexe argilo-humique (Fig. 1).
Lorsque l'on chaule, on veut à la fois neutraliser les hydrogènes de la solution du sol et ceux, beaucoup plus nombreux, qui sont sur le CAH. Seul le pH tampon permet de déterminer les quantités de chaux à ajouter (voir la section Module 10 Chaulage).
Valeurs cibles du pH eau
Le pH eau ciblé pour la majorité des cultures en sol minéral est généralement entre 6,0 et 7,0. Parmi les légumes, la pomme de terre fait exception avec un pH visé entre 5,2 à 6,2. À noter que dans les sols organiques on cherche à atteindre des pH plus faibles, soit entre 5 et 5,8.
La valeur du pH eau à viser varie selon la texture de sol, particulièrement entre les sols sableux ou fins (loameux et argileux). Les valeurs à viser sont les suivantes (ref. Anne Weill) :
- sol sableux : 6,0 à 6,5 ;
- loam : 6,2 à 6,7 ;
- sol argileux : 6,3 à 7.
Pour la majorité des légumes, le pH eau critique minimal est 5,5, sans quoi des toxicités à l’aluminium et au manganèse peuvent survenir, en plus d’inhiber la fixation symbiotique de l’azote pour les légumineuses. Un pH eau au-dessus de 7 diminue la disponibilité de certains oligo-éléments (Fe, Mn, Zn, Cu).
Pour certaines cultures acidophiles, comme le bleuet ou la canneberge, on vise un pH eau entre 4,0 ou 4,5 à 5,0.
Il est important de corriger le pH eau afin d’assurer un solubilisation adéquate des éléments nutritifs et favoriser une activité microbiologique maximale du sol. Les microorganismes doivent être actifs pour assurer la minéralisation de l’azote organique. De plus, le calcium a un effet structurant sur les sols. Pour savoir comment ajuster le pH eau, consulter la section chaulage.
Matière organique
La matière organique est formée de l’ensemble des molécules du sol contenant du carbone provenant des organismes vivants ou en cours de décomposition, principalement des plantes mais aussi des microorganismes et des animaux comme les vers de terre. Elle est composée de substances facilement biodégradables (molécules simples provenant de matière végétale ayant un faible rapport C/N ou microorganismes) et molécules complexes difficilement dégradables (lignine, résines). L’analyse de sol standard permet de connaître la quantité totale de carbone dans le sol. La matière organique totale du sol est ensuite calculée avec l’équation suivante: MO totale (%) = C total (en %) X 1,724.
Au Québec, le taux de matière organique des sols minéraux se situe en moyenne entre 3 à 5 %. Les valeurs à rechercher pour les sols minéraux sont les suivantes :
- sol sableux : > 3 %;
- loam : > 3,5 %;
- sol argileux : > 4 %
Une partie de cette matière organique se minéralise assez rapidement. Cette fraction, appelée fraction active ou labile, peut être évaluée dans certains laboratoires (POXC= Permanganate Oxidizable Carbon) en plus des analyses standard. Plusieurs études scientifiques ont montré que les sols riches en carbone labile produisent plus de nitrate (NO3). Ces études démontrent ainsi l’effet stimulant du carbone labile sur l’activité biologique des sols, un meilleur développement des plantes et prélèvement du phosphore, la nutrition et le rendement des cultures (Culman et coll. 2013, Landry 2011).
La minéralisation de la matière organique contribue à la nutrition azotée des cultures. Le sol fournit en général 50% de l’azote nécessaire aux plantes (Tran, 1996). Bien que l’évaluation de la contribution en azote de la matière organique peut être évaluée de plusieurs façon, le Guide du CRAAQ 2013 suggère de considérer un apport de 15 kg N/ha pour chaque 1% de teneur en matière organique du sol au-dessus de 4%, jusqu’à 7 % (soit un maximum de 45 kg/ha/année) dans les sols travaillés. Par contre, lorsque l’activité biologique est réduite, ce chiffre peut être plus bas et même nul, ce qui est à considérer lors du calcul de la fertilisation à apporter. En effet, un sol minéral riche en matière organique peut parfois résulter d’une faible activité microbiologique causée par exemple par des sols froids, compactés ou mal drainés. Dans ces conditions, la matière organique s’accumule au lieu de se décomposer.
En agriculture biologique, on cherche à optimiser la minéralisation de la matière organique pour nourrir les plantes. Il faut ensuite compenser les pertes de matière organique dans les rotations. Les apports d’amendements organiques (fumiers, compost), l’utilisation d’engrais verts ou cultures de couvertures incluant les prairies permettent de préserver le carbone des sols. Une fertilisation basée uniquement sur des granules de fumier de volaille ou d’autres fertilisants comme la poudre de sang ou de la farine de plume apporte peu de matière organique au sol ce qui entraîne une baisse du taux de matière organique et de la fertilité à moyen-long terme.
Nouvelles information sur la dynamique de la matière organique
La matière organique a longtemps été divisée en plusieurs classes dont celles des acides fulviques, des acides humiques et de l’humine. Ces substances ont été obtenues par extraction chimique mais n’ont n'ont pas été observées dans le sol (Lehmann et Kleber, 2015). Un ensemble de recherches plus récentes a permis de mieux comprendre la matière organique et son interaction avec la matière minérale (Cotrufo et al. 2013, Lavalle et Cotrufo, 2020). La matière organique a été divisée en deux parties :
- la matière organique associées aux minéraux d’une durée de vie de 10 à 1000 ans
- la matière organique particulaire d’une durée de vie 1 à 50 ans.
La matière organique associées aux minéraux provient principalement de l’apport de substrats labiles (matière végétale jeune riche en azote contenant peu de lignine) facilement utilisable par les micro-organismes. Elle est sous forme de polymères microbiens et végétaux et de leur produits de dégradation et sont fortement liés à la matière minérale. Ce sont ces liens organo-minéraux qui permettent la stabilisation de la matière organique.
La matière organique particulaire provient des résidus végétaux riches en lignine et pauvres en azote. Cette matière organique est moins stable car elle est utilisée moins efficacement par les micro-organismes. Sa conversion en carbone organique stable est plus lente que pour la fraction précédente.
Phosphore et indice de saturation en phosphore (ISP)
L’analyse de sol permet de connaître les quantités de phosphore soluble, disponibles pour les plantes. Ces quantités ne constituent qu’une fraction du phosphore total contenu dans les sols. Le phosphore est fortement fixé au fer, à l’aluminium et au manganèse en sol acide et aux carbonates de calcium et de magnésium en sol calcaire. L’efficacité de l'absorption du phosphore par les plantes est mauvaise en sol acide. Des indices (aussi appelés taux) de saturation en phosphore (ISP) ont été développés afin de favoriser une fertilisation basée sur la biodisponibilité du phosphore et éviter la surfertilisation en phosphore des sols. Ces indices sont basés sur l’extraction du phosphore avec la méthode Mehlich-III dans les sols acides et neutres du Québec. En dehors du Québec, les sols alcalins sont généralement analysés avec la méthode Olsen pour estimer le phosphore biodisponible.
Il y a trois indices différents pour exprimer la disponibilité du phosphore aux plantes:
- L’ISP1 est basé uniquement sur le phosphore (P) et l’aluminium (Al) : ISP1 (%) = (P/Al) x 100. Il est utilisé dans tous les sols minéraux sauf dans le cas de la canneberge.
- L’ISP2 est utilisé dans les sols minéraux cultivés en canneberge et tient compte du fer (Fe) en plus de l’aluminium : ISP2 (%) = (P/31 / (Al/27 + Fe/56)) x100.
- L’ISP3 est utilisé dans les sols organiques. Il est basé sur le phosphore, l’aluminium et le fer avec un facteur pour optimiser la faible disponibilité du Fe avec l’extraction Mehlich-III : ISP3 (%) = ((P/31 / (Al/27+ 5 x Fe/56)) x 100.
L'interprétation des niveaux de phosphore doit se faire à l’aide des grilles de fertilisation qui sont présentées dans la section 14.2.2. Des observations faites sur le terrain pour les sols de texture moyenne indiquent que des valeurs ISP1 entre 2,6 % et 6,5 %, dans les sols de moins de 30 % d’argile, sont optimales pour la majorité des légumes. Des carences en phosphore peuvent survenir dans des sols à texture moyenne et légère avec un ISP1 inférieur 1,5 %, particulièrement au moment de la germination des semences.
Pour l’ensemble des sols minéraux, les valeurs environnementales maximales ont été déterminées pour les sols excessivement riches en phosphore selon la texture de sol (Tableau 1). Au-delà de ces valeurs, les sols sont considérés saturés en phosphore et les recommandations en phosphore ne devraient pas dépasser les exportations par les récoltes afin de réduire les teneurs en phosphore des sols saturés.
Tableau 1. Valeurs critiques environnementales des sols minéraux (ISP1 critique)
| Sol à teneur en argile ⩽ 30% | 13,1% |
| Sols à teneur en argile >30% | 7,6% |
Avec l’historique de surfertilisation en phosphore dans plusieurs régions du Québec, les sols saturés en phosphore sont une réalité qui peut ajouter une complexité lorsque vient le temps de répondre aux besoins en azote des cultures, tout en conciliant les normes environnementales en vigueur. L’indice de saturation des sols en phosphore a un impact majeur sur la gestion du phosphore sur l’entreprise, impliquant le choix des rotations, des amendements organiques et des fertilisants à utiliser.
Aluminium
La teneur du sol en aluminium (Al) est une caractéristique du sol. Elle permet d’estimer la capacité qu’a un sol de fixer le phosphore et de savoir, dans une certaine mesure, si un sol est podzolique (sol de faible potentiel, sableux, très acide et riche en fer et aluminium) (Tableau 2). Au Québec, les sols peuvent fixer de 400 à 10 000 kg/ha de phosphore (Tran et Giroux, 19901980) et, par conséquent, le rendre non disponible pour les plantes. Le fer et l’aluminium sont les principaux facteurs responsables de cette fixation; plus le pH est bas (acide), plus ces deux éléments fixent solidement le phosphore. Les podzols fixent beaucoup de phosphore, car ils sont riches en fer et en aluminium.
Tableau 2 : Capacité de fixation du phosphore en fonction du type de sol
| Capacité de fixation | Type de sol | Teneur du sol en Al (ppm) |
| Faible | Variable | < 1 100 |
| Moyenne | Variable | 1 100-1 600 |
| Élevée | Typique des sols sableux podzoliques | >1 600 |
Source : CRAAQ, 2003
Potassium
La richesse en potassium des sols est fortement liée à la texture. Les sols argileux sont généralement naturellement riches en potassium et les sols sableux sont naturellement pauvres, les loams étant intermédiaires.
Les niveaux de richesse sont présentés au tableau 3 afin de permettre de se situer lors de la lecture de l’analyse de sol.
Tableau 3 : Niveaux de richesse des sols en potassium pour les cultures horticoles
| Résultat de l'analyse (kg/ha) | |
| Catégorie | Potassium (K) |
| Sol très pauvre | 0 – 100 |
| Sol pauvre | 101 - 200 |
| Sol moyen | 201 - 300 |
| Sol bon | 301 - 400 |
| Sol riche | 401 - 500 |
| Sol très riche | 501 - 600 |
| Sol excessivement riche | > 601 |
Adapté de CRAAQ, 2013
L'interprétation des niveaux de potassium doit se faire à l’aide des grilles de fertilisation qui sont présentées dans la section 14.2.3.
Calcium et magnésium
Le niveau de calcium des sols dépend de la texture de sol et des historiques d’apports en chaux. En général, au Québec, plus le pH est élevé pour une texture donnée, plus le niveau de calcium est élevé. D’autre part, pour un même pH, plus le sol est argileux, plus le niveau de calcium est élevé.
Le niveau de magnésium dépend beaucoup de la texture de sol. Les argiles sont plus riches en magnésium que les sols sableux. En général, il n’y a pas de risque de carence en magnésium dans les sols lourds. Dans les sols légers, il y a des risques de carence en magnésium lorsque le niveau de magnésium est inférieur à 200 kg/ha, en particulier si une fertilisation importante en potassium est réalisée.
Tableau 4. Influence de la texture de sol sur les niveaux de calcium et de magnésium des sols au Québec
| Texture du sol | Niveau de calcium attendu (kg/ha) avec une bonne gestion du chaulage | Niveau de magnésium typique (kg/ha) 1 |
| Sol sableux | 2 000 à 4 000 | <300 |
| Loam | 4 000 à 7 000 | 300-700 |
| Sol argileux | >7 000 | >700 |
- Les données concernant le magnésium sont valables pour la plupart des sols au Québec, mais ne constituent pas une règle absolue.
Capacité d’échange cationique
La capacité d’échange cationique (CEC) correspond à la capacité du sol à stocker les cations (calcium, magnésium, potassium, ions hydrogènes, etc.). Il s’agit d’une mesure de l’ensemble des charges négatives qui se trouvent sur l’argile et la matière organique et qui peuvent retenir les cations. La CEC dépend principalement de la texture du sol (Tableau 3); plus le sol contient d’argile, plus la CEC est élevée et plus il peut stocker les éléments nutritifs. La matière organique a aussi une influence sur la CEC; plus le sol contient de matière organique, plus la CEC est élevée. Cela explique pourquoi la CEC d’un sol organique est très élevée. Les sols à faible CEC ont une faible capacité de rétention des cations.
Dans les rapports d’analyse de sol, la CEC est calculée (et non mesurée) à partir du pH tampon et des niveaux de calcium, de potassium et de magnésium. Un chaulage important, ou encore les sols calcaires peuvent donc fausser ce calcul.
| Texture du sol | CEC (meq/100 g) |
| Sol sableux | <12 |
| Loam | 13-24 |
| Sol argileux | 25-35 |
| Sol organique | 50-200 |
Pourcentages en saturation
Le pourcentage en saturation en bases est calculé pour le calcium, le magnésium et le potassium. Il s'agit du pourcentage de la CEC occupé par l'élément en question. Le pourcentage de saturation en calcium visé dépend de la texture de sol. Il aide à déterminer si les niveaux de calcium sont adéquats selon le type de sol. Les valeurs du tableau ci-dessous peuvent être utilisées comme balises pour aider à déterminer si des corrections en calcium sont nécessaires.
Tableau 5 : Niveau de calcium visé dans le sol, selon la texture du sol
| Texture du sol | Niveau de calcium attendu (kg/ha) avec une bonne gestion du chaulage | Pourcentage de saturation en calcium attendu (%) |
| Sol sableux | 2 000 à 4 000 | 55-60 |
| Loam2 | 4 000 à 7 000 | 60-70 |
| Sol argileux | >7 000 | >703 |
Il y a un antagonisme entre le potassium et le magnésium. Par exemple, lorsque le sol n’est pas riche en potassium, un apport important de magnésium peut entraîner une carence en potassium et vice-versa. Il n’est pas possible de se baser sur le ratio K/Mg pour prédire un problème.Toutefois, il est tout à fait normal dans les sols argileux d’avoir 4 à 7 fois plus de magnésium que de potassium alors que cette situation peut être très problématique en sol sableux. Un apport important de chaux dolomitique en sol léger pourrait augmenter le risque de carence en potassium si le sol est pauvre en potassium et si une fertilisation adéquate en potassium n’est pas prévue.
Oligo-éléments
Les oligo-éléments, aussi appelés éléments mineurs ou éléments traces, sont des éléments nécessaires aux plantes en très petites quantités.
En terre minérale, les principaux oligo-éléments à surveiller sont le bore (B), le molybdène (Mo), le zinc (Zn) et le manganèse (Mn). En terre organique, il faut aussi surveiller le cuivre (Cu). Le tableau 7 permett d’interpréter les résultats d’analyse de sol en ce qui concerne les oligo-éléments. L’extraction Mehlich III est utilisée pour le zinc, le manganèse et le cuivre. L’extraction à l’eau chaude est utilisée pour le bore et le molybdène. Les laboratoires effectuent une extraction Mehlich III pour le bore si la méthode d’extraction à l’eau chaude n’est pas spécifiquement demandée. Les résultats de l’extraction Mehlich III pour le bore ne peuvent pas être interprétés, car la marge d’erreur est trop élevée.
Tableau 7 : Interprétation des résultats d’analyse de sol en ce qui concerne les oligo-éléments en terre minérale (ppm)
| Oligo-élément | Niveau | Seuil de carence en deçà duquel il faut effectuer un apport | ||
| Bas | Moyen | Bon | ||
| Molybdène1 | <0,1 | 0,1-0,2 | 0,2 et plus | < 0,2 ppm : apport requis |
| Bore1 | 0,8-1,1 | < 1,1 ppm (cultures exigeantes); < 0,7 cultures modérément exigeantes | ||
| Cuivre2 | 0-0,3 | 0,3-0,6 | 0,6 et plus | < 0,6 ppm : apport requis |
| Cuivre, terres noires2 | 0-30 | Non précisé | ||
| Manganèse2 | 0-5 | 6-11 | 12 et plus | pH < 6,5 : aucune application
pH > 6,5 et Mn < 11 ppm : apport requis |
| Zinc2 | 0-1,8 | 1,9-2,8 | 2,8 et plus | pH < 6,5 : < 1 ppm: apport requis
pH > 6,5 et Zn < 1,9 ppm : apport requis |
- Extraction à l’eau chaude. L’extraction Mehlich III n’est pas calibrée pour le bore et le molybdène.
- Extraction Mehlich III.
Source : CRAAQ, 2013. Note: ces données ne sont pas spécifiques pour les légumes.
Aucun mot clé.
- ↑ La méthode Mehlich-III a été développée en 1984 par l'américain Adolph Mehlich, un scientifique des sols de la Caroline du Nord (Mylavarapu, 2020). Elle fut implantée au Québec en 1989 par le Service de recherches en sols du ministère de l'Agriculture, des Pêcheries et de l'Alimentation du Québec (MAPAQ). Elle permet d'extraire plusieurs éléments nutritifs pour les sols dont le pH est acides à neutres, ce qui correspond à la plupart des sols agricoles du Québec (Parent, 2021). La solution Mehlich-III, un acide faible, a été élaboré de façon à imiter les conditions d'extraction des éléments nutritifs dans la zone racinaire. Lors de l'analyse, la solution est versée sur l'échantillon de sol qui se trouve dans un entonnoir. Le liquide qui en ressort est analysé pour en connaître le contenu en divers éléments (P, K, Ca, Mg, Na, Al, Cu, Zn, Mn et Fe). La solution extractive Mehlich III se compose de CH3COOH, NH4NO3, NH4F, HNO3 et EDTA (MELCCFP, s. d.)